-

Терапевтичні підходи в онкології
Сучасна онкологія базується на трьох основних методах впливу на злоякісні пухлини: хіміотерапії, радіотерапії та імунотерапії. Кожен із цих підходів має свої механізми дії, показання та характерні побічні ефекти. У низці випадків їх застосовують у комбінації для підвищення ефективності лікування і зниження ризику рецидиву. Нижче розглянуто ключові особливості кожного з терапевтичних методів, а також принципи…
-

Основи онкологічної діагностики
Точна і своєчасна діагностика злоякісних пухлин – основний фактор успіху в онкології. Сучасні методи обстеження дають змогу не тільки виявити новоутворення на ранній стадії, а й точно визначити його гістологічний тип, оцінити ступінь поширеності та вибрати оптимальний план лікування. В арсеналі онкологів-радіологів і патологів ключове місце посідають біопсія, комп’ютерна томографія і гібридне дослідження ПЕТ-КТ.…
-
Професійний догляд у разі захворювань ясен
Захворювання ясен потребують комплексного підходу, який об’єднує домашні методи догляду та професійні процедури, що проводяться в клініці. Пародонтологічна гігієна спрямована на видалення бактеріального нальоту і зубного каменю, усунення запальних вогнищ і створення умов для відновлення тканини пародонту. Сучасні клініки доповнюють механічну обробку апаратними технологіями, включно з лазерною терапією, яка прискорює регенерацію ясен і знижує…
-

Терапія за пародонтозу в пародонтолога
Пародонтоз, або хронічне захворювання пародонту, характеризується руйнуванням опорної тканини зуба, що веде до розхитування і втрати зубів. Сучасні методики лікування спрямовані на зупинку запального процесу, відновлення балансу мікрофлори порожнини рота і регенерацію кісткової та сполучної тканини. Ключову роль у цьому відіграє пародонтолог, який підбирає індивідуальну програму терапії з поєднанням консервативних і за необхідності хірургічних…
-
Етапи встановлення зубної коронки
Встановлення коронки на зуб – серйозна стоматологічна процедура, що дає змогу відновити значно зруйновану коронкову частину, повернути жувальну функцію та естетичний зовнішній вигляд. Щоб результат був довговічним і надійним, кожен етап роботи повинен виконуватися строго за протоколом. Нижче докладно описано всі основні стадії процесу: від первинної консультації та діагностики до фінішного полірування і подальшого…
-
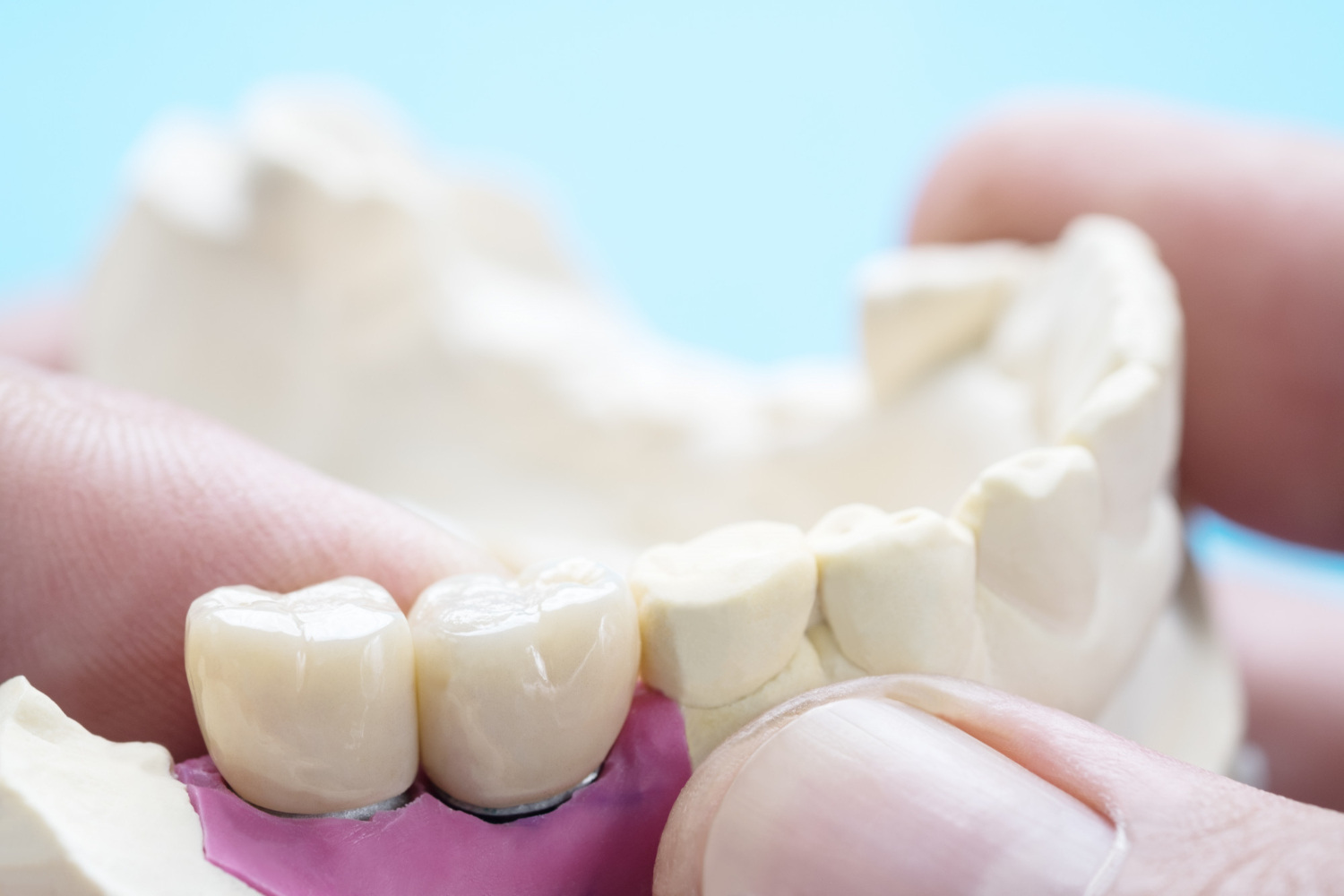
Коли показані зубні коронки
Встановлення коронки є однією з найпоширеніших реставраційних процедур у сучасній стоматології. Коронка дає змогу відновити анатомічну форму, жувальну функцію та естетику зуба в разі значної втрати твердих тканин, після ендодонтичного лікування або під час протезування мостоподібними конструкціями. Вибір матеріалу коронки і технології її виготовлення залежить від клінічної ситуації, вимог до міцності і зовнішнього вигляду,…
-

Як проходить лікування елайнерами
Виправлення прикусу і вирівнювання зубів за допомогою прозорих капп-елайнерів – це сучасний спосіб ортодонтичної корекції, що поєднує естетику, комфорт і передбачуваність результату. Терапія проводиться за планом, розрахованим за допомогою тривимірних технологій, і дає змогу пацієнтові помітити поступове вирівнювання зубів без використання класичних брекетів. Весь процес можна умовно розділити на кілька етапів, від первинної консультації…
-

Переваги елайнерів перед брекетами
Прозорі капи-елайнери в сучасній ортодонтії стають дедалі більш затребуваними завдяки поєднанню естетики, комфорту та прогнозованості результату. На відміну від традиційних металевих або керамічних брекет-систем, вони вирішують завдання вирівнювання зубного ряду більш щадним методом. Нижче ми розповімо про ключові переваги елайнерів, які роблять їх привабливим вибором для багатьох пацієнтів. Практично невидимий апарат Елайнери виготовляються з…
